« Neuigkeiten
Wissenschaftler entdecken möglichen neuen Therapieansatz
von
Sandra Michme
Wissenschaftler am Institut für Klinische Chemie und Pathobiochemie des Universitätsklinikums Magdeburg berichten im internationalen Fachjournal Nature Communication erstmals über einen möglichen neuen Therapieansatz für einer der am meisten gefürchteten Komplikationen nach einer hämatopoetischen Stammzelltransplantation (HSCT).
Die HSCT ermöglicht heutzutage eine effiziente Therapie vieler maligner Erkrankungen, zum Beispiel des blutbildenden Knochenmarks, zu denen u.a. auch Leukämien gehören. Die HSCT führt aber häufig zu einer Erkrankung, die einer Autoimmunerkrankung des ganzen Körpers gleicht und gravierende und durchaus auch tödliche Folgen für die Patienten haben kann.
Diese als "Graft versus Host Disease (GvHD)" bekannte Erkrankung ist für einen großen Teil der Patienten nicht behandelbar. Die Autoren zeigen in ihrer Studie einen möglichen neuen Therapieansatz auf: die Gerinnungsprotease aktiviertes Protein C (aPC) kann diese gefährliche Reaktion stoppen.
Die aktuellen Ergebnisse basieren auf neuen Einblicken in die Regulation von Immunzellen. "Wir konnten erstmals zeigen, dass das Blutgerinnungssystem direkt die Immunantwort reguliert. Damit konnten wir einen neuen Mechanismus, durch den das Immunsystem kontrolliert wird, nachweisen. Wir denken, dass diese Ergebnisse die Grundlage für neue Therapien immunologischer Erkrankungen, wie der GvHD, sein könnten", so Prof. Dr. med. Berend Isermann, Leiter der Studie und Direktor des Instituts für Klinische Chemie und Pathobiochemie an der Medizinischen Fakultät der Otto-von-Guericke-Universität Magdeburg. "Diese Erkenntnisse ändern unser Verständnis des gesamten Gebietes drastisch, da wir einen neuen Mechanismus, der einen fehlgeleitete Immunantwort kontrollieren kann, nachweisen konnten", sagt Dr. Satish Ranjan, Erstautor der Studie, der zusammen mit den Koautoren die experimentellen Arbeiten durchgeführt hat.
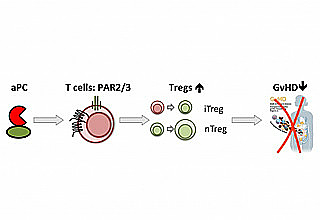
Die aktuellen Befunde legen nahe, dass aPC die Aktivierung und Differenzierung der T Zellen durch direkte Interaktion mit den T Zellen moduliert. Die Präinkubation der T Zellen mit aPC verhindert die Aktivierung allogener T Zellen, welche die GvHR verstärken. Auch stimuliert aPC die Differenzierung regulatorischer T Zellen, die vor der GvHD schützen. Entscheidend für einen möglichen klinischen Nutzen ist, dass der therapeutische Effekt der T Zellen gegen die Tumorzellen (der sogenannte Graft-versus-Leukämie Effekt) erhalten bleibt. Diese wichtigen Arbeiten wurden in einem Mausmodellen mit menschlichen T Zellen bestätigt. "Der nächste Schritt ist jetzt eine klinische Pilotstudie. Wir führen bereits Diskussionen mit Kollegen aus der Klinik und der Industrie", so Prof. Isermann. Dr. Ranjan fügt hinzu: "Dies ist ein wichtiger Schritt auf dem Weg zur Entwicklung neuer Therapien für Patienten, die an GvHD leiden. Insbesondere für Patienten, bei denen die Standardtherapie mit Steroiden nicht wirkt, könnten davon profitieren".
Diese wichtigen neuen Erkenntnisse wurden im Rahmen einer Studie des SFB854 (Sonderforschungsbereich 854, von der DFG gefördert) an der Medizinischen Fakultät der Otto-von-Guericke-Universität Magdeburg erhoben. Der SFB854, dessen Sprecher Prof. Dr. med. Burkhart Schraven, Direktor des Instituts für Molekulare und Klinische Immunologie, ist, hat die Erforschung der inter- und intrazelluläre Zell-Zell Kommunikation im Immunsystem zum Ziel. Der SFB854 ist eng mit dem Gesundheitscampus (GCI3) assoziiert und hat mehrere Landmarkstudien in den letzten Jahren hervorgebracht.
Die HSCT ermöglicht heutzutage eine effiziente Therapie vieler maligner Erkrankungen, zum Beispiel des blutbildenden Knochenmarks, zu denen u.a. auch Leukämien gehören. Die HSCT führt aber häufig zu einer Erkrankung, die einer Autoimmunerkrankung des ganzen Körpers gleicht und gravierende und durchaus auch tödliche Folgen für die Patienten haben kann.
Diese als "Graft versus Host Disease (GvHD)" bekannte Erkrankung ist für einen großen Teil der Patienten nicht behandelbar. Die Autoren zeigen in ihrer Studie einen möglichen neuen Therapieansatz auf: die Gerinnungsprotease aktiviertes Protein C (aPC) kann diese gefährliche Reaktion stoppen.
Die aktuellen Ergebnisse basieren auf neuen Einblicken in die Regulation von Immunzellen. "Wir konnten erstmals zeigen, dass das Blutgerinnungssystem direkt die Immunantwort reguliert. Damit konnten wir einen neuen Mechanismus, durch den das Immunsystem kontrolliert wird, nachweisen. Wir denken, dass diese Ergebnisse die Grundlage für neue Therapien immunologischer Erkrankungen, wie der GvHD, sein könnten", so Prof. Dr. med. Berend Isermann, Leiter der Studie und Direktor des Instituts für Klinische Chemie und Pathobiochemie an der Medizinischen Fakultät der Otto-von-Guericke-Universität Magdeburg. "Diese Erkenntnisse ändern unser Verständnis des gesamten Gebietes drastisch, da wir einen neuen Mechanismus, der einen fehlgeleitete Immunantwort kontrollieren kann, nachweisen konnten", sagt Dr. Satish Ranjan, Erstautor der Studie, der zusammen mit den Koautoren die experimentellen Arbeiten durchgeführt hat.
Die aktuellen Befunde legen nahe, dass aPC die Aktivierung und Differenzierung der T Zellen durch direkte Interaktion mit den T Zellen moduliert. Die Präinkubation der T Zellen mit aPC verhindert die Aktivierung allogener T Zellen, welche die GvHR verstärken. Auch stimuliert aPC die Differenzierung regulatorischer T Zellen, die vor der GvHD schützen. Entscheidend für einen möglichen klinischen Nutzen ist, dass der therapeutische Effekt der T Zellen gegen die Tumorzellen (der sogenannte Graft-versus-Leukämie Effekt) erhalten bleibt. Diese wichtigen Arbeiten wurden in einem Mausmodellen mit menschlichen T Zellen bestätigt. "Der nächste Schritt ist jetzt eine klinische Pilotstudie. Wir führen bereits Diskussionen mit Kollegen aus der Klinik und der Industrie", so Prof. Isermann. Dr. Ranjan fügt hinzu: "Dies ist ein wichtiger Schritt auf dem Weg zur Entwicklung neuer Therapien für Patienten, die an GvHD leiden. Insbesondere für Patienten, bei denen die Standardtherapie mit Steroiden nicht wirkt, könnten davon profitieren".
Diese wichtigen neuen Erkenntnisse wurden im Rahmen einer Studie des SFB854 (Sonderforschungsbereich 854, von der DFG gefördert) an der Medizinischen Fakultät der Otto-von-Guericke-Universität Magdeburg erhoben. Der SFB854, dessen Sprecher Prof. Dr. med. Burkhart Schraven, Direktor des Instituts für Molekulare und Klinische Immunologie, ist, hat die Erforschung der inter- und intrazelluläre Zell-Zell Kommunikation im Immunsystem zum Ziel. Der SFB854 ist eng mit dem Gesundheitscampus (GCI3) assoziiert und hat mehrere Landmarkstudien in den letzten Jahren hervorgebracht.
weitere Informationen :
zur Pressemeldung
Article Nature Communications
SFB854
